研究プロジェクト:TRAP displayによる人工抗体の創製
人工抗体とは?
疾患に対する治療法の1つに抗体医薬品があります。抗体とは、免疫グロブリンというタンパク質の一種で、特定の標的を認識して結合します。例えば、がん細胞表面に存在するタンパク質を標的とした抗体医薬品は、標的タンパク質を認識して結合することで、がん細胞を死滅させることが可能です。抗体医薬品は、治療効果が高く副作用が少ないことが特徴で、有効な治療法が確立されていない難病に対する治療が期待できます。しかし、抗体はサイズが大きく構造が複雑であることから、製造にコストがかかることが知られています。そこで近年は、抗体よりもサイズが小さい「低分子抗体」が抗体の代替ツールとして注目されています。低分子抗体とは、免疫グロブリンよりも小さいタンパク質で、抗体のように特定の標的に結合できるタンパク質を指します。この低分子抗体は、免疫のシステムを利用せず、人工的に設計することができるため、我々はこれを人工抗体と呼んでいます。
TRAP displayとは?
これまで、多くの人工抗体が報告されてきました。フィブロネクチンというタンパク質を骨格としたMonobody [1] や、リポカリンというタンパク質を骨格としたAnticalin [2] が代表的です。人工抗体を創製するには、骨格とするタンパク質を選び、そのタンパク質が目的の標的に結合するように改造することが必要です。タンパク質はアミノ酸が繋がってできています。そのため、タンパク質を構成しているアミノ酸を、別のアミノ酸に置き換えることで改造することができます。しかし、アミノ酸は天然で20種類も存在するため、どのアミノ酸に置き換えたら良いか、さらにはどの位置のアミノ酸を置き換えたら良いか、判断することができません。そこで、様々な箇所を様々なアミノ酸にランダムに置き換えて大量の人工抗体の候補を作製し、その中から標的に結合する人工抗体を選び出す方法 (スクリーニング, セレクション) が有効です。
1997年に報告されたmRNA display [3, 4] は、10^13種類もの人工抗体の中から、目的の人工抗体を選び出すことができる技術です。しかしこの技術では、人工抗体の選択に必要な操作の煩雑さと所用時間の長さを欠点としています。そこで我々は、mRNA displayをより簡便かつ迅速化したTRanscription-TRanslation coupled with Association of Puromycin-linker (TRAP) displayを開発しました。現在、このTRAP displayを用いて、様々な標的に対する人工抗体の創製に取り組んでいます。
主要論文の解説
T. Ishizawa, T. Kawakami, P. C. Reid, H. Murakami*, TRAP display: a high-speed selection method for the generation of functional polypeptides.
J. Am. Chem. Soc. 2013, 135, 5433-5440.
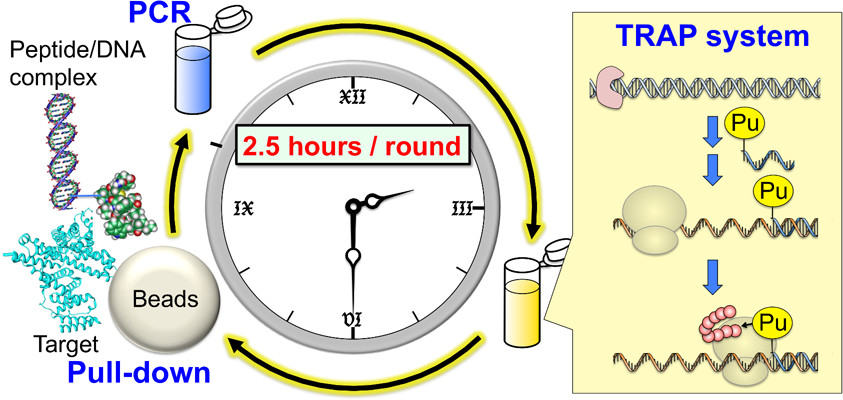
https://doi.org/10.1021/ja312579umRNA displayをより簡便かつ迅速化したTRanscription-TRanslation coupled with Association of Puromycin-linker (TRAP) displayが開発されました。この論文では、特定の標的に結合する環状ペプチドの選択を報告しています。
mRNA displayによるペプチドのセレクションには約2〜3週間必要ですが、TRAP displayでは約1〜2日間で終えることができます。このTRAP displayの開発は、ペプチドの選択を高速化し、様々な分子の創出に貢献すると期待されます。
T. Kondo, Y. Iwatani, K. Matsuoka, T. Fujino, S. Umemoto, Y. Yokomaku, K. Ishizaki, S. Kito, T. Sezaki, G. Hayashi, H. Murakami*, Antibody-like proteins that capture and neutralize SARS-CoV-2.
Sci. Adv., 2020, 6(42), eabd3916.
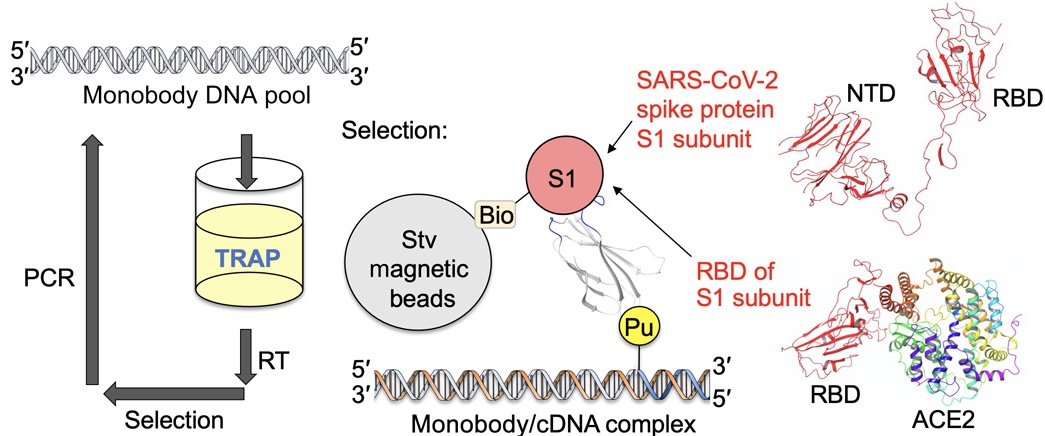
https://doi.org/10.1126/sciadv.abd3916TRAP displayをさらに改良し、人工抗体 (Antibody-like protein) のセレクションを可能にしました。また、当時流行していた新型コロナウイルスSARS-CoV-2に対する人工抗体Monobodyを創製しました。
我々は、SARS-CoV-2のReceptor binding domain (RBD) を標的としました。RBDはSARS-CoV-2の表面上に存在するスパイクタンパク質の一部であり、ヒト細胞の表面にあるAngiotensin-converting enzyme 2 (ACE2) と結合することが報告されています。そのため、RBDに結合できるMonobodyを創製することができれば、SARS-CoV-2がヒト細胞内に取り込まれるのを防ぐことができるため、新型コロナウイルスの感染を阻害することができます。
TRAP displayによるセレクションの結果、RBDに非常に強く結合するMonobody (結合解離定数 0.42-1.9 nM) を、わずか4日間で取得することに成功しました。TRAP displayは、パンデミックを引き起こすウイルスをはじめとする様々な標的に対して、人工抗体の迅速な創製を可能にする革新的な技術です。
S. Umemoto, T. Kondo, T. Fujino, G. Hayashi, H. Murakami*, Large-scale analysis of mRNA sequences localized near the start and amber codons and their impact on the diversity of mRNA display libraries.
Nucleic Acids Res., 2023, 51, 7465-7479.
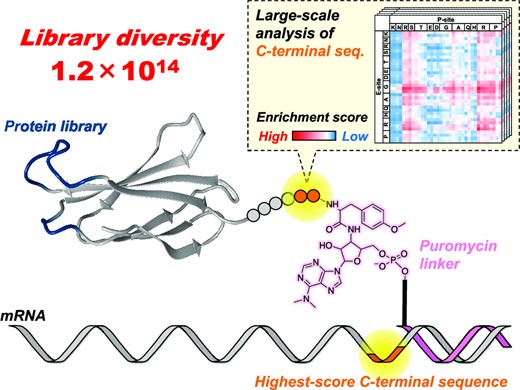
https://doi.org/10.1093/nar/gkad555TRAP displayでは、まず人工抗体の設計図であるDNAをランダム化することによって、様々なDNAが集まった「DNAライブラリ」を構築します。その後、DNAライブラリをTRAP systemに加えることによって、DNAからmRNAへの転写・Puromycinという物質との連結・人工抗体の翻訳合成 (mRNAの情報をもとに人工抗体が作られること) が連続して進行します。Puromycinは、翻訳合成された人工抗体の末端と共有結合を形成する性質を有するため、mRNA/Puromycin-人工抗体という複合体が作製されます。これにより、人工抗体とその設計図であるmRNAを対応づけることが可能となり、標的に結合できる人工抗体の情報をmRNAの配列から知ることができるのです。
そのため、TRAP displayでは人工抗体とmRNAが対応づけられていることが非常に重要です。mRNAと対応づけられていない人工抗体は、回収されても情報を読むことができません。mRNAと対応づけられている人工抗体の数を増やすことで、より広い範囲から人工抗体を選び出すことができるようになり、選ばれる人工抗体の親和性 (どれだけ強く結合することができるか) を向上させられることが報告されています。[5] この論文では、mRNA/Puromycin-人工抗体複合体の形成効率を向上させることで、TRAP displayによって高親和性の人工抗体を選択できる可能性を高めました。
T. Kondo, M. Eguchi, S. Kito, T. Fujino, G. Hayashi, H. Murakami.*, cDNA TRAP display for rapid and stable in vitro selection of antibody-like proteins.
Chem. Commun., 2021, 57, 2416-2419.
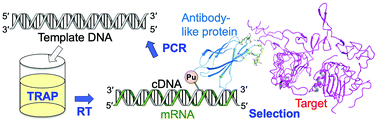
https://doi.org/10.1039/D0CC07541H前述した通り、TRAP displayでは人工抗体とmRNAが対応づけられていることが重要です。しかし、mRNAはRNase (リボヌクレアーゼ) によって分解されることが知られています。RNaseは空気中の微生物や人間の皮膚・髪・唾液に存在するため、実験系へのコンタミネーションが容易に起こり得ます。また、細胞や血清中にもRNaseは存在するため、TRAP displayでは、細胞を標的としたセレクションや、血清中で機能する人工抗体のセレクションが不可能です。
mRNA displayを改良し、RNase存在下でのセレクションを可能にしたのがcDNA display [6-8] です。我々はその戦略に倣い、TRAP displayを改良して「cDNA TRAP display」を開発しました。これにより、様々な条件で安定なセレクションを迅速に行うことができるようになりました。
G. Hayashi*, T. Naito, S. Miura, N. Iwamoto, Y. Usui, M. Bando-Shimizu, S. Suzuki, K. Higashi, M. Nonaka*, S. Oishi*, H. Murakami*, Generating a mirror-image monobody targeting MCP-1 via TRAP display and chemical protein synthesis.
Nat. Commun., 2024, 15, 10723.
https://doi.org/10.1038/s41467-024-54902-xTRAP displayなどのセレクション手法では人工抗体を翻訳によって合成しますが、このとき、通常はL体のアミノ酸で構成されるL体の人工抗体が合成されます。しかし、体内のタンパク質はL体であるため、L体の人工抗体はそれらによって認識されやすく、分解を受けたり、異物として認識されて免疫によって排除されたり (免疫原性) します。一方、L体の人工抗体を鏡写しにしたD体の人工抗体は、体内で認識されにくいという利点があります。そのため、効果的な医薬品を開発するためには、人工抗体を「D体のアミノ酸」で合成し、体内のL体の標的に結合するD体の人工抗体を創製するのが有効です。しかし、翻訳ではD体の人工抗体を合成することが困難であるため、新たな戦略が必要でした。
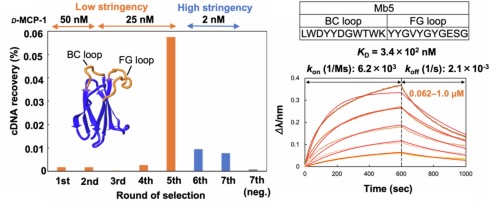
そこで、標的をD体のアミノ酸で化学合成し、「D体」の標的に結合する「L体」の人工抗体をセレクションによって取得した後、取得した人工抗体をD体のアミノ酸で化学合成することによって、「L体」の標的に結合する「D体」の人工抗体を創製する戦略が考案されました。[9] 我々はこれをTRAP displayに応用し、D体のMCP-1 (Monocyte chemoattractant protein-1) に結合するL体の人工抗体Monobodyを取得した後、それをD体のアミノ酸で化学合成し、L体のMCP-1に結合するD体のMonobodyを取得することに成功しました。この戦略により、D体の人工抗体による、治療効果の高い医薬品の創製が加速されると期待できます。
参考文献
[1] A. Koide, C. W. Bailey, X. Huang, S. Koide, The fibronectin type III domain as a scaffold for
novel binding proteins. J. Mol. Biol., 1998, 284, 1141-1151.
[2] G. Beste, F. S. Schmidt, T. Stibora, A. Skerra, Small antibody-like proteins with prescribed
ligand specificities derived from the lipocalin fold. Proc. Natl. Acad. Sci. USA, 1999, 96, 1898-1903.
[3] R. W. Roberts, J. W. Szostak, RNA-peptide fusions for the in vitro selection of peptides and
proteins. Proc. Natl. Acad. Sci. USA, 1997, 94, 12297-12302.
[4] N. Nemoto, E. Miyamoto-Sato, Y. Husimi, H. Yanagawa, In vitro virus: Bonding of mRNA bearing
puromycin at the 3'-terminal end to the C-terminal end of its encoded protein on the ribosome in vitro.
FEBS Lett. 1997, 414, 405-408.
[5] G. Kamalinia, B. J. Grindel, T. T. Takahashi, S. W. Millward, R. W. Roberts, Directing evolution
of novel ligands by mRNA display. Chem. Soc. Rev. 2021, 50, 9055-9103.
[6] M. Kurz, K. Gu, A. Al-Gawari, P. A. Lohse, cDNA-protein fusions: Covalent protein–gene conjugates for the in vitro selection of peptides and proteins. ChemBioChem, 2001, 2, 666–672.
[7] I. Tabuchi, S. Soramoto, N. Nemoto, Y. Husimi, An in vitro DNA virus for in vitro protein evolution. FEBS Lett. 2001, 508, 309–312.
[8] J. Yamaguchi, M. Naimuddin, M. Biyani, T. Sasaki, M. Machida, T. Kubo, T. Funatsu, Y. Husimi, N. Nemoto, cDNA display: a novel screening method for functional disulfide-rich peptides by solid-phase synthesis and stabilization of mRNA–protein fusions. Nucleic Acids Res. 2009, 37, e108.
[9] T. N. M. Schumacher, L. M. Mayr, D. L. Minor, Jr., M. A. Milhollen, M. W. Burgess, P. S. Kim, Identification of d-Peptide Ligands Through Mirror-Image Phage Display. Science, 1996, 271, 1854-1857.